четвер, 25 грудня 2014 р.
понеділок, 22 грудня 2014 р.
Увага!!! Визначено дати проведення ЗНО.
Увага!
Визначено дати проведення тестів ЗНО у 2015 році
Основна сесія зовнішнього незалежного оцінювання у 2015 році відбудеться у червні 2015 року, а загальнообов’язкове тестування випускників шкіл з української мови і
літератури у квітні.
Відповідно до календарного плану проведення ЗНО, що затверджений Міністерством освіти і науки, основна сесія зовнішнього незалежного оцінювання розпочнеться 3 червня тестом з французької мови та завершиться 26 червня тестуванням з хімії. За цей період, випускники шкіл
2015 року, а також минулих років, які вирішать продовжити здобуття освіти у вищих навчальних закладах, матимуть можливість скласти від одного до трьох з 11 запропонованих тестових предметів.
Загально обов’язковий тест з української мови і літератури буде проведено
24 квітня.
Результати тестування, які одночасно зараховуватимуться як
результати державної підсумкової атестації за курс повної загальної середньої освіти для всіх випускників старшої школи, будуть оголошені до 15 травня.
До 20 травня школи отримають від Українського центру оцінювання якості освіти відомості з результатами державної підсумкової атестації з української мови своїх випускників.
Іншою особливістю проведення ЗНО у 2015 році є виділення окремих днів для
проведення тестувань з іноземних мов.
Нагадаємо, у попередні роки зовнішнє оцінювання з іноземних мов
проводилося в один день, а абітурієнти мали можливість обрати лише один тест з чотирьох іноземних мов.
До 6 квітня абітурієнти отримають запрошення перепустки для участі у
зовнішньому незалежному оцінювання з української мови і літератури,
запрошення на інші тестування надійдуть до 20 травня. Оголошення
результатів тестування абітурієнтів, які складатимуть тести ЗНО під
час основної сесії відбуватиметься починаючи з 16 червня.
Ті з учасників, хто з об’єктивних причин не матиме можливості скласти тести під час основної сесії тестування, зможуть скласти тести під час додаткової сесії, що відбудеться у період з 9 червня до 9 липня. Реєстрація
абітурієнтів для участі у зовнішньому незалежному оцінювання
здійснюватиметься регіональними центрами оцінювання якості
освіти у період з 5 січня до 20 лютого 2015 року. Загалом, учасники
ЗНО матимуть можливість скласти не більше чотирьох тестів з
переліку предметів ЗНО, до якого включено 12 навчальних предметів:
українська мова і література, історія України, математика, біологія, географія,
фізика, хімія, а також англійська, німецька, французька,
іспанська та російська мови. Тести з української мови і літератури, а також
математики матимуть два рівні складності.
Календар проведення зовнішнього незалежного оцінювання абітурієнтів у 2015 році:
українська мова і література -24 квітня 2015 року (п’ятниця);
французька мова – 03 червня 2015 року (середа);
німецька мова – 05 червня 2015 року (п’ятниця);
іспанська мова – 08 червня 2015 року (понеділок);
англійська мова – 10 червня 2015 року (середа);
математика – 12 червня 2015 року (п’ятниця);
російська мова – 15 червня 2015 року (понеділок);
біологія – 17 червня 2015 року (середа);
історія України – 19 червня 2015 року (п’ятниця);
фізика – 22 червня 2015 року (понеділок);
географія – 24 червня 2015 року (середа);
хімія – 26 червня 2015 року (п’ятниця).
Кисень.Озон.Цікава інформація
Кисень. Озон. Цікава інформація
Фізичні властивості речовин, утворених елементом Оксигеном
Атоми Оксигену можуть утворювати два типи молекул: O2 — кисень та O3 — озон.
Явище існування кількох простих речовин, утворених атомами одного хімічного елемента, називається алотропією. А прості речовини, утворені одним елементом, називають алотропними модифікаціями.
Отже, озон і кисень — це алотропні модифікації елемента Оксигену.
Властивості
|
Кисень
|
Озон
|
Формула сполуки
|
O2
|
O3
|
Зовнішній вигляд у звичайних умовах
|
Газ
|
Газ
|
Колір
|
У парах кисень безбарвний. Рідкий — блідо-блакитного кольору, а твердий — синього
|
Пари озону світло-синього кольору. Рідкий — синього кольору, а твердий являє собою темно-фіолетові кристали
|
Запах і смак
|
Без запаху й смаку
|
Різкий характерний запах (у малих концентраціях надає повітрю запаху свіжості)
|
Температура плавлення
|
-219 °С
|
-192 °С
|
Температура кипіння
|
-183 °С
|
-112 °С
|
Густина при н. у.
|
1,43 г/л
|
2,14 г/л
|
Розчинність уводі
|
4 об’єми кисню в 100 об’ємах води
|
45 об’ємів озону в 100 об’ємах води
|
Магнітні властивості
|
Рідкий і твердий кисень — парамагнітні речовини, тобто втягуються в магнітне поле
|
Має діамагнітні властивості, тобто не взаємодіє з магнітним полем
|
Біологічна роль
|
Необхідний для дихання рослин і тварин (у суміші з азотом або інертним газом). Вдихання чистого кисню призводить до сильного отруєння
|
В атмосфері утворює так званий озоновий шар, який захищає біосферу від шкідливого впливу ультрафіолетового випромінювання. Отруйний
|
Хімічні властивості кисню й озону
Взаємодія кисню з металами
Молекулярний кисень — досить сильний окисник. Він окислює практично всі метали (окрім золота й платини). Багато металів повільно окислюються на повітрі, але в атмосфері чистого кисню згорають дуже швидко, при цьому утворюється оксид:
Однак деякі метали при горінні утворюють не оксиди, а пероксиди (у таких сполуках ступінь окиснення Оксигену дорівнює -1) або надпероксиди (ступінь окиснення атома Оксигену — дробова). Прикладом таких металів можуть бути барій, натрій та калій:

Взаємодія кисню з неметалами
Оксиген проявляє ступінь окиснення -2 в сполуках, які утворені з усіма неметалами, окрім Флуору, Гелію, Неону та Аргону. Молекули кисню при нагріванні безпосередньо вступають у взаємодію з усіма неметалами, окрім галогенів та інертних газів. В атмосфері кисню самозаймається фосфор та деякі інші неметали:
При взаємодії кисню із фтором утворюється оксиген фторид, а не фтор оксид, оскільки атом Фтору має більшу електронегативність, аніж атом Оксигену. Оксиген фторид — це газ блідо-жовтого кольору. Його використовують як дуже сильний окисник та фторувальний агент. У цій сполуці ступінь окиснення Оксигену дорівнює +2.
У надлишку фтору може утворюватися диоксиген дифторид, в якому ступінь окиснення Оксигену дорівнює +1. За будовою така молекула схожа на молекулу гідроген пероксиду.
За певних умов кисень вступає у взаємодію з багатьма складними речовинами. При цьому утворюються оксиди елементів або прості речовини, утворені цими елементами:
Кисень може вступати у взаємодію з оксидами, в яких елементи перебувають не у вищих ступенях окиснення:
Озон є більш сильним окисником, аніж молекулярний кисень. Майже всі реакції, які проходять під дією кисню, проходять також з озоном, але при цьому реакція протікає швидше й виділяється більша кількість енергії. Багато речовин під дією озону займаються:

При взаємодії калію з озоном утворюється озонід (сполука іонного типу):
Озон виявляють у лабораторних умовах пропусканням досліджуваної суміші через розчин калій йодиду з невеликою кількістю крохмалю:
Якщо в пропущеній газовій суміші присутній озон, то розчин забарвлюється в інтенсивно-синій колір, за рахунок утворення комплексної сполуки йоду з крохмалем. Цю реакцію називають якісною реакцією на озон.
Кисень в аналогічну реакцію не вступає.
Кисень зазвичай добувають у лабораторіях електролізом слабкого водного розчину натрій гідроксиду (електроди нікельовані):
Кисень можна добути термічним розкладанням багатих на Оксиген сполук (хлоратів, перманганатів, нітратів, пероксидів, оксидів):

У промисловості кисень добувають із рідкого повітря. Спочатку повітря охолоджують до -200 °С, а потім поступово нагрівають. При -196 °С випаровується азот, і залишається рідкий кисень.
Методи добування озону
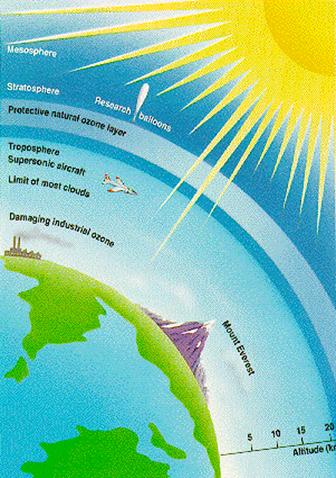
Озон утворюється в атмосфері на висоті 20— 30 кілометрів з кисню під дією ультрафіолетового випромінювання Сонця.
Озон можна добути з кисню під дією тліючого електричного розряду.
Він також утворюється в різних копіювальних апаратах, при зварюванні металів, при роботі трансформаторів та при ударі блискавки.
Застосування кисню й озону. Значення озонового шару
Кисень використовують усі аеробні живі істоти для дихання. У процесі фотосинтезу рослини виділяють кисень і поглинають вуглекислий газ.
Молекулярний кисень застосовують для так званої інтенсифікації, тобто прискорення окисних процесів у металургійній промисловості. А ще кисень використовують для добування полум’я з високою температурою. При горінні ацетилену (С2Н2) в кисні температура полум’я сягає +3500 °С. У медицині кисень застосовують для полегшення дихання хворих. Його також використовують у дихальних апаратах для роботи людей у важкій для дихання атмосфері. Рідкий кисень застосовують як окисник ракетного палива.
Озон використовують у лабораторній практиці як дуже сильний окисник. У промисловості з його допомогою дезінфікують воду, оскільки йому притаманна сильна окисна дія, яка знищує різні мікроорганізми.
Пероксиди, надпероксиди та озоніди лужних металів застосовують для регенерації кисню в космічних кораблях та на підводних човнах, Таке застосування засноване на реакції цих речовин з вуглекислим газом СО2:
У природі озон міститься у високих шарах атмосфери на висоті близько 20—25 км, у так званому озоновому шарі, що захищає Землю від жорсткого сонячного випромінювання. Зменшення концентрації озону в стратосфері хоча б на 1 може призвести до важких наслідків, таких зростання числа онкологічних захворювань шкіри в людей і тварин, збільшення числа захворювань, пов’язаних із пригніченням імунної системи людини, уповільнення росту наземних рослин, зниження швидкості росту фітопланктону тощо.
Без озонового шару життя на планеті було б неможливим. Тим часом забруднення атмосфери різними промисловими викидами призводять до руйнування озонового шару. Найнебезпечнішими речовинами для озону є фреони (їх використовують як холодоагенти в холодильних машинах, а також як наповнювачі для балончиків з дезодорантами) та відходи ракетного палива.
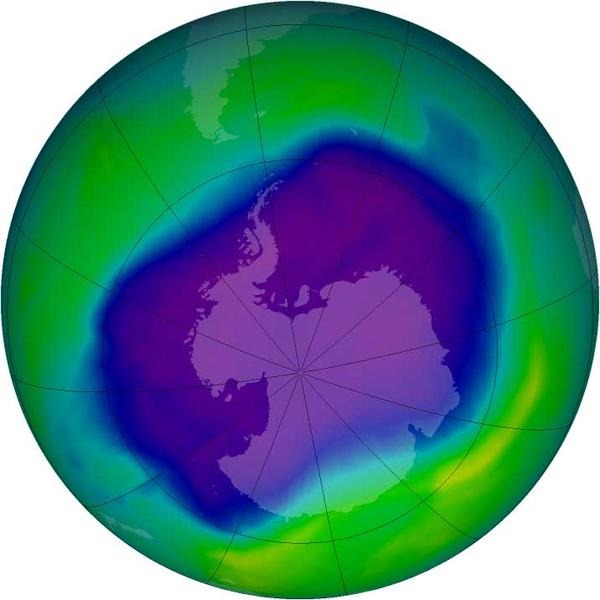
Світове співтовариство було дуже стурбоване у зв’язку з утворенням діри в озоновому шарі на полюсах нашої планети, у зв’язку із чим у 1987 р. був прийнятий «Монреальський протокол щодо речовин, які руйнують озоновий шар», котрий обмежив використання речовин, шкідливих для озонового шару.
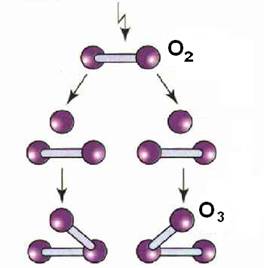
Схема утворення озону з кисню
Схема утворення озону з кисню
Озон у рідкому агрегатному стані-це фіолетова вибухонебезпечна речовина
Підписатися на:
Коментарі (Atom)